ETERES:
los éteres presentan un
pequeño momento dipolar neto (por
ejemplo, 1.18 D para
el dietil éter).
Esta polaridad débil no
afecta apreciablemente a los puntos de ebullición
de los éteres, que son similares a los de los alcanos de pesos moleculares comparables y mucho más bajos que los de los alcoholes
isómeros. Comparemos, por ejemplo, los puntos de ebullición del n-heptano (98ºC), el metil
pentil éter (100ºC) y el alcohol hexílico (157ºC). Los puentes de hidrógeno
que mantienen firmemente unidas las
moléculas de alcoholes
los éteres presentan un
pequeño momento dipolar neto (por
ejemplo, 1.18 D para
el dietil éter).
Esta polaridad débil no
afecta apreciablemente a los puntos de ebullición
de los éteres, que son similares a los de los alcanos de pesos moleculares comparables y mucho más bajos que los de los alcoholes
isómeros. Comparemos, por ejemplo, los puntos de ebullición del n-heptano (98ºC), el metil
pentil éter (100ºC) y el alcohol hexílico (157ºC). Los puentes de hidrógeno
que mantienen firmemente unidas las
moléculas de alcoholes
propiedades químicas :
Los éteres tienen muy poca reactividad química, debido a la
dificultad que presenta la ruptura del enlace C—O. Por ello, se utilizan
mucho como disolventes inertes en reacciones orgánicas.
En contacto con el aire
sufren una lenta oxidación en la que se forman peróxidos muy inestables y poco
volátiles. Estos constituyen un peligro cuando se destila un éter, pues se
concentran en el residuo y pueden dar lugar a explosiones. Esto se evita
guardando el éter con hilo de sodio o añadiendo una pequeña cantidad de un
reductor (SO4Fe, LiAIH4) antes de la destilación.
Los éteres no son reactivos a
excepción de los epóxidos. Las reacciones de los epóxidos pasan por la apertura
del ciclo. Dicha apertura puede ser catalizada por ácido o apertura mediante
nucleófilo.
En contacto con el aire
sufren una lenta oxidación en la que se forman peróxidos muy inestables y poco
volátiles. Estos constituyen un peligro cuando se destila un éter, pues se
concentran en el residuo y pueden dar lugar a explosiones. Esto se evita
guardando el éter con hilo de sodio o añadiendo una pequeña cantidad de un
reductor (SO4Fe, LiAIH4) antes de la destilación.
Los éteres no son reactivos a
excepción de los epóxidos. Las reacciones de los epóxidos pasan por la apertura
del ciclo. Dicha apertura puede ser catalizada por ácido o apertura mediante
nucleófilo.
Reacciones de los éteres. Escisión por ácidos
Los éteres
son compuestos relativamente poco reactivos.
La unón éter
es muy estable en relación con
las bases, los agentes oxidantes y los reductores. En lo que respecta a la unión éter, estas sustancias sólo dan un tipo de reacción, que es la escisión
por ácidos:
La escisión procede sólo
en condiciones bastante enérgicas: se necesitan ácidos
concentrados (por lo general H
o HBr) y temperaturas elevadas.
Inicialmente, un alquil éter da un halogenuro de alquilo
y un alcohol, el cual puede seguir
reaccionando para formar un segundo halogenuro de alquilo. Debido a la baja reactividad del enlace entre el oxígeno y el anillo aromático, un alquil aril éter sufre ruptura del enlace alquilo-oxígeno y produce un fenol y un halogenuro de alquilo. Por ejemplo:
La escisión implica un ataque nucleofílico del ion
halogenuro sobre el éter protonado, con desplazamiento de la débilmente básica molécula de alcohol:
Dicha reacción se produce con
mayor facilidad que la del desplazamiento del ion alcóxido fuertemente básico del éter
neutro.
La reacción de un éter protonado con un ion
halogenuro puede proceder, al igual que la de un alcohol
protonado, por medio de un mecanismo SN1,
O por un mecanismo SN2,
Dependiendo de las condiciones y de la estructura del éter. Como es de suponer, un grupo alquilo primario tiende
a sufrir un desplazamiento por SN2, mientras que uno terciario tiende a hacerlo por SN1.Dependiendo de las condiciones y de la estructura del éter. Como es de suponer, un grupo alquilo primario tiende
a sufrir un desplazamiento por SN2, mientras que uno terciario tiende a hacerlo por SN1.
obtencion de los eteres
Los éteres alifáticos simétricos pueden obtenerse por
deshidratación de alcoholes , mediante la acción del ácido sulfúrico. Este es
uno de los métodos comerciales de preparación del éter ordinario, dietiléter,
por lo que se llama frecuentemente éter sulfúrico.Se lleva a cabo tratando el alcohol
con ácido sulfúrico a 140°. La deshidratación es intermolecular:
| H2SO4
140º
| H2O + CH3—CH2—O—CH2CH3 |
| etanol | dietiléter |
Este proceso se ve fácilmente afectado por reacciones
secundarias, como la formación de sulfatos de alquilo (especialmente si baja la
temperatura), y la formación de olefinas (especialmente si sube la
temperatura).
La deshidratación de alcoholes puede también realizarse en
fase vapor, sobre alúmina a 300°, aunque este procedimiento sólo es
satisfactorio con alcoholes primarios, ya que los secundarios y los terciarios
dan lugar a la formación de olefinas.
A partir de alcoholatos (Síntesis de Williamson)
Los alcoholatos dan lugar a la formación de éteres al ser
tratados con halogenuros de alquilo según:
| IR’ | R—O—R’ + NaI | |
| alcoholato | halogenuro de alquilo | éter | |
USOS PRINCIPALES
suelen ser utilizados como anestésicos, son sustancias que
duran poco a temperatura ambiente, puesto que se evaporan con fácilidad casi
como un alcohol etílico pero son más rápidos. pueden ser nocivos para la salud
si se administran en dosis masivas.
- Medio para extractar para concentrar ácido acético y otros
ácidos.
- Medio de arrastre para la deshidratación de alcoholes etílicos e isopropílicos.
- Disolvente de sustancias orgánicas (aceites, grasas, resinas, nitrocelulosa, perfumes y alcaloides).
- Combustible inicial de motores Diésel.
- Fuertes pegamentos
- Desinflamatorio abdominal para despues del parto, exclusivamente uso externo.
-Es llamado la medicina antigua porque en la antiguedad se usaba como anestesico, debido a que no existian los metodos de anestesia moderna.
uso en lo medicinal :
- Medio de arrastre para la deshidratación de alcoholes etílicos e isopropílicos.
- Disolvente de sustancias orgánicas (aceites, grasas, resinas, nitrocelulosa, perfumes y alcaloides).
- Combustible inicial de motores Diésel.
- Fuertes pegamentos
- Desinflamatorio abdominal para despues del parto, exclusivamente uso externo.
-Es llamado la medicina antigua porque en la antiguedad se usaba como anestesico, debido a que no existian los metodos de anestesia moderna.
uso en lo medicinal :
El éter dietílico es un buen anestésico. Es seguro para el
paciente, ya que el pulso cardiaco y respiratorio, así como
la presión
arterial, permanecen normales durante su aplicación, la cual
además
es muy sencilla. Sus desventajas estriban en los efectos
lateral que
produce, como náuseas e irritación de las vías
respiratorias.





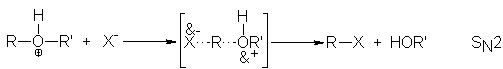
No hay comentarios:
Publicar un comentario